BlueBird罕见血液疾病药物LentiGlobin获突破性治疗药物资格 ...
www1.sdfyy.cn/yjkweb/Web/aspx/yjkInfo.aspx?InfoID...
轉為繁體網頁
3 days ago - 美国FDA授予BlueBird Bio公司血液疾病药物LentiGlobin突破性治疗药物资格,从而可以加快这款治疗 ... 主办单位:苏州大学附属第一医院药学部.
www1.sdfyy.cn/yjkweb/Web/aspx/yjkInfo.aspx?InfoID...
轉為繁體網頁
3 days ago - 美国FDA授予BlueBird Bio公司血液疾病药物LentiGlobin突破性治疗药物资格,从而可以加快这款治疗 ... 主办单位:苏州大学附属第一医院药学部.药学行业动态:让蓝鸟继续飞:基因疗法LentiGlobin BB305获 ...
www.yaojia.org › 药学论坛 › 产业经济 › 行业动态 - 轉為繁體網頁
2月2日, BLUEBIRD公司正式宣布,他们的LentiGlobin BB305被FDA授予突破性疗法认定为地中海贫血病的 ... 2015-2-4 09:23| 发布者: 药学助手| 查看: 7| 评论: 0 ...
www.yaojia.org › 药学论坛 › 产业经济 › 行业动态 - 轉為繁體網頁
2月2日, BLUEBIRD公司正式宣布,他们的LentiGlobin BB305被FDA授予突破性疗法认定为地中海贫血病的 ... 2015-2-4 09:23| 发布者: 药学助手| 查看: 7| 评论: 0 ...【快訊】藥品上市加速,BLUE大漲4.88%
www.chinesefn.com/m1/de.chtml?id=1211999&xxid=0.6044113
2015年5月19日 - 生物制藥公司Bluebirdbio((BLUE))用於治療地中海貧血癥(beta-thalassemia major)
www.chinesefn.com/m1/de.chtml?id=1211999&xxid=0.6044113
2015年5月19日 - 生物制藥公司Bluebirdbio((BLUE))用於治療地中海貧血癥(beta-thalassemia major)Bluebird基因療法LentiGlobin BB305獲得FDA突破性療法認證
big.sunyet.com › 生物基因 › 生物研究 › 基因研究
2015年2月5日 - 而在稍早時候,制藥巨頭羅氏公司也獲得了FDA授予其開發的PD-L1 ... title for LentiGlobin BB305 as a new treatment for beta-thalassemia major, ...
big.sunyet.com › 生物基因 › 生物研究 › 基因研究
2015年2月5日 - 而在稍早時候,制藥巨頭羅氏公司也獲得了FDA授予其開發的PD-L1 ... title for LentiGlobin BB305 as a new treatment for beta-thalassemia major, ...Bluebird新型罕见贫血症药物LentiGlobin BB305临床研究再 ...
www.hanjianbing.org/content/details_11_2117.html
轉為繁體網頁
2014年12月16日 - Bluebird公司最近透露,公司开发的用于治疗一种罕见遗传性血液疾病--重型β-
www.hanjianbing.org/content/details_11_2117.html
轉為繁體網頁
2014年12月16日 - Bluebird公司最近透露,公司开发的用于治疗一种罕见遗传性血液疾病--重型β-bluebird bio, Inc. - 財經百科- 財經知識庫- MoneyDJ理財網
www.moneydj.com/KMDJ/Wiki/WikiViewer.aspx?KeyID...b865...
... 養症的Lenti-D,現已進入phase II/III期研究;以及LentiGlobin,主要用於治療β型地中海貧血及鐮刀型貧血的LentiGlobin,在 ... 藥華藥C肝新藥向TFDA遞交三期臨床.
www.moneydj.com/KMDJ/Wiki/WikiViewer.aspx?KeyID...b865...
... 養症的Lenti-D,現已進入phase II/III期研究;以及LentiGlobin,主要用於治療β型地中海貧血及鐮刀型貧血的LentiGlobin,在 ... 藥華藥C肝新藥向TFDA遞交三期臨床.《药学实践杂志》
www.yxsjzz.cn/ch/reader/more_news_list.aspx?...id...
轉為繁體網頁
利用抗生素消除癌症干细胞, 2015-03-22, 159. 基因疗法LentiGlobin BB305获FDA
www.yxsjzz.cn/ch/reader/more_news_list.aspx?...id...
轉為繁體網頁
利用抗生素消除癌症干细胞, 2015-03-22, 159. 基因疗法LentiGlobin BB305获FDAmhoman - Guestbook
mhoman.eu/page14.php?SessionID=529e63a254e0ed21de7eb
2015年3月4日 - ... 和心情鬱悶,請諮詢您的醫療保健提供者或藥劑師的藥是否會導致問題。 ... 藍鳥生物期望與FDA提交IND在2014年評估LentiGlobin患者SCDIn ...
mhoman.eu/page14.php?SessionID=529e63a254e0ed21de7eb
2015年3月4日 - ... 和心情鬱悶,請諮詢您的醫療保健提供者或藥劑師的藥是否會導致問題。 ... 藍鳥生物期望與FDA提交IND在2014年評估LentiGlobin患者SCDIn ...疑夕的微博- 微博台灣站
tw.weibo.com/bzq1123?page=9
這篇論文的給藥方法是瘤內注射,瘤內注射很容易引起炎症,附帶引起部分癌細胞的死亡, ... 疑夕評美股# BLUE的基因療法LentiGlobin再下一城,對鐮狀細胞貧血病.
tw.weibo.com/bzq1123?page=9
這篇論文的給藥方法是瘤內注射,瘤內注射很容易引起炎症,附帶引起部分癌細胞的死亡, ... 疑夕評美股# BLUE的基因療法LentiGlobin再下一城,對鐮狀細胞貧血病.主題:IPO | 醫源世界 - 大
big5.39kf.com/my/tag_1_79a80a73/
... 公司2014年12月發布了其罕見貧血癥藥物LentiGlobin BB305的最新進展數據。 ... Regado公司:IPO后,Regado的抗凝血藥Revolixys在3期臨床試驗中連續出現 ...
big5.39kf.com/my/tag_1_79a80a73/
... 公司2014年12月發布了其罕見貧血癥藥物LentiGlobin BB305的最新進展數據。 ... Regado公司:IPO后,Regado的抗凝血藥Revolixys在3期臨床試驗中連續出現 ...让蓝鸟继续飞:基因疗法LentiGlobin BB305获FDA突破性疗法认证!
 什么是地中海贫血病? 地中海贫血是一组遗传性溶血性贫血疾病。由于遗传的基因缺陷致使血红蛋白中一种或一种以上珠蛋白链合成缺少或不足所导致的贫血或病理状态。缘于基因缺陷的复杂性与多样性,使缺乏的珠蛋白链类型、数量及临床症状变异性较大。 β地中海贫血(地贫)是一种常见的单基因遗传病,致使β珠蛋白合成减少或完全不能合成,从而导致过剩的不稳定的α链形成。大多数重型β地贫都要靠输血维持生命,这一方面给家庭和社会带来巨大的经济负担,另一方面长期输血不能根本治愈患者,并造成一系列与输血有关的疾病,最终威胁患者的生命,长久以来,人们寄希望于基因治疗。 什么是LentiGlobin BB305基因治疗方案? Bluebird公司方面为FDA做出的这一决定表示雀跃。这一方面再次奠定了公司在基因疗法方面领跑者的地位,另一方面也向市场表明了向患者体内输送修正基因以治疗疾病的可行性和安全性。 LentiGlobin BB305是利用慢病毒载体将修正后的β-球蛋白基因导入到由患者体内分离而来的造血干细胞中,然后将这些基因重组的造血干细胞经过扩增再回输至患者体内,以恢复患者正常合成血红蛋白的能力。这一疗法能够使地中海贫血患者彻底摆脱输血维持的局面。而就在去年12月份,Bluebird公司在美国血液学会上公布了接受这种疗法的四名患者已经在未输血治疗的条件下正常生活了三个月以上。 该疗法的简要治疗原理:在病人体外通过一种病毒将正确的基因替换掉病人本来就有的坏掉基因。Bluebird公司通过Lentiviral病毒用正确的把天生的坏掉的基因在病人的造血干细胞中替换掉,替换以后,再输入病人体内,然后,病人的这个血液病就好了。具体看下面的图。 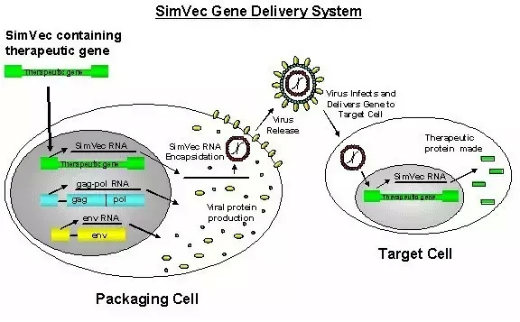 突破性疗法认定 2012年7月9日,《FDA安全与创新法案》(Food and Drug Administration Safetyand Innovation Act)正式实施,FDA第四条特别审批通道诞生,即突破性药物(Breakthrough Therapies)。在2013年,FDA至少收到141份突破性药物资格(breakthrough therapy designation,BTD)申请,而这些申请中有37项获得授权,其中4个新药(Kalydeco、Gazyva、Imbruvica、Sovaldi)经该通道上市。 FDA (美国国家药监局)设计突破性疗法认定的目的在于加速创新药物的研发,主要针对严重威胁生命的药物的研发。Breakthroughtherapy designation需要初步的数据支持:这个新药可以极大程度的提高病人的状况。这个是新药审批的快速通道。 拓展阅读: Gene therapy pioneer bluebird bags a 'breakthrough' title for lead program |





No comments:
Post a Comment